초점
"CAR-T보다 낫다" 컬럼비 등 이중항체 신약 대세 부상
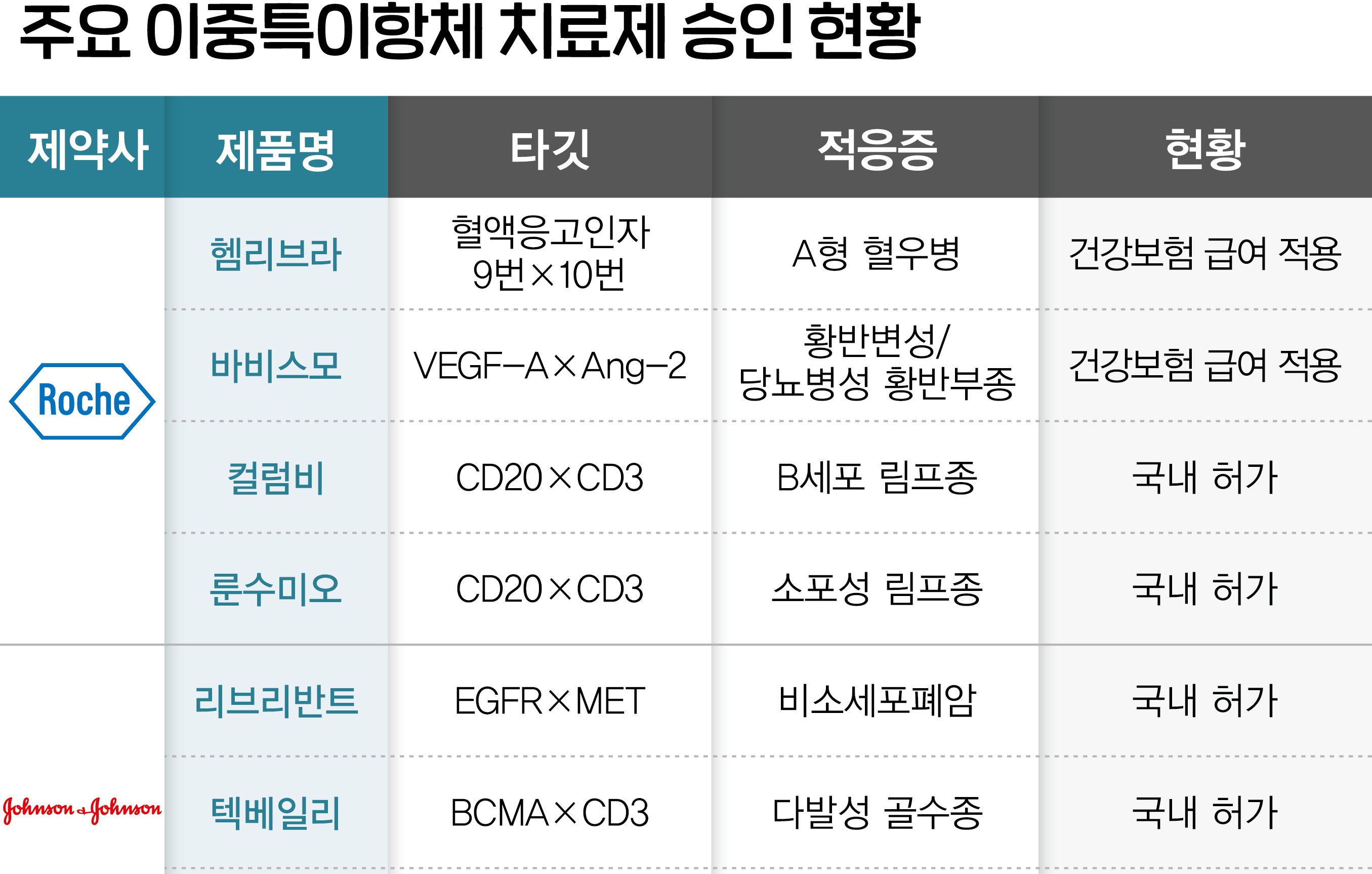
메디칼타임즈=문성호 기자컬럼비 등 이중특이항체 기반 치료제가 글로벌 항암제 시장에서 대세로 자리 잡으며 급부상하고 있다.고형암 분야에서 항체약물접합체(Antibody Drug Conjugate, ADC)가 기대를 모으고 있다면 혈액암 분야에서는 이중특이항체 기반 항암제가 대세로 부상하며 임상 현장에서 각광을 받고 있는 것.이로 인해 실제 임상 현장에서는 이미 혈액암 등 일부 질환에서 활용 중인 CAR-T 치료제를 대신할 것이라고 전망도 나오고 있다. 국내 제약․바이오 업계에서도 이중특이항체 기반 치료제 개발에 열을 올리는 이유다.혈액암 대세 이중특이항체 치료제3일 제약업계에 따르면, 최근 주요 글로벌 제약사들의 이중특이항체 기반 항암제가 미국 FDA와 혹은 국내 식품의약품안전처 허가를 받으며 임상현장에서 본격 활용되고 있는 것으로 확인됐다.이중항체(Bispecific antibody)는 두 개의 서로 다른 항원(Antigen)을 인식, 동시에 결합할 수 있는 항체를 말한다. 기존 한 개 항원만을 타깃 하는 항체치료제도 우수한 효과가 나타났지만, 매우 복잡하고 다양한 요인으로 발생하는 암을 잡기엔 한계가 있었다. 이중항체는 이러한 한계를 극복, 두 개의 항원 간의 상호작용을 조절하거나 한 번에 여러 개의 활성을 조절해 더욱 강력한 효과를 낼 수 있다. 주요 글로벌 제약사 이중특이항체 기반 치료제 개발 및 허가 현황이다.현재 글로벌 현재 글로벌 시장에서는 ▲로슈 룬수미오(모수네투주맙), 컬럼비(글로피타맙), 헴리브라(에미시주맙), 바비스모(파리시맙) ▲얀센 리브리반트(아미반타맙), 텍베일리(테클리스타맙) ▲애브비 엡킨리(엡코리타맙) ▲화이자 엘렉스피오(엘라나타맙) 등이 허가돼 있다.이들 글로벌 제약사들의 치료제는 적응증이 다르지만 이중특이항체 기반으로 개발됐다는 것이 공통점이다.특히 최근 들어서는 혈액암 분야에서 이중특이항체 기반 항암제들이 임상현장에서 쓰임새를 넓히고 있다. 이중 로슈 CD20xCD3 T세포 관여 이중특이항체 기반 항암제인 룬수미오(모수네투주맙)와 컬럼비(글로피타맙)는 최근 국내 식약처 허가를 통해 임상현장에서 활용이 가능한 상태다.여기서 룬수미오는 지난해 10월 두 가지 이상의 전신 치료 후 재발성 또는 불응성 소포성 림프종(Follicular Lymphoma, FL) 성인 환자 치료에 국내 허가됐다. 컬럼비는 지난달 7일 두 가지 이상 전신치료 후 재발성 또는 불응성 미만성 거대 B세포 림프종(Diffuse Large B-Cell Lymphoma, DLBCL) 치료제로 국내 허가됐다. DLBCL은 신체를 보호하는 B세포가 통제할 수 없이 성장하거나 증식하는 질환으로 1~2차 치료요법에 실패한 환자에게 3차 치료옵션이 제한적인 상황에서 컬럼비가 대안이 될 것으로 기대받고 있다.존슨앤드존슨 텍베일리 제품사진.또한 존슨앤드존슨(이하 J&J)의 다발성 골수종 치료제로 이중특이항체 기반 치료제 '텍베일리(테클리스타맙)'도 국내 허가를 받아 주목을 받고 있다. 텍베일리는 국내에서 J&J 측이 50여명 환자를 대상으로 무상 공급 프로그램(Early Access Program, EAP)을 진행한 것으로 알려진 상태다.EAP를 통해 50명 환자를 대상으로 텍베일리 투여가 이뤄지면서 국내 대학병원 중심 혈액종양내과 의료진 사이에서 그 효과를 둘러싼 다양한 의견이 오가고 있다는 후문.이 같이 국내에도 본격적으로 이중특이항체 기반 항암제들이 혈액암을 중심으로 임상현장에서 활용되기 시작하면서 기대감이 커지고 있는 상황.대한혈액학회 차기 이사장인 삼성서울병원 김석진 교수(혈액종양내과)는 "FL은 잦은 재발이 특징인 지연성 비호지킨 림프종"이라며 "후속 치료가 진행될수록 PFS가 감소하는 특징이 있다"고 평가했다.김석진 교수는 "약 26%의 FL 환자가 항CD20 항체+화학요법 초기치료 후 불응성 또는 조기 재발하는 것을 보였다"며 "그간 1, 2차 치료에 실패하거나 반복되는 재발을 경험하는 환자들을 위한 보다 효과적인 3차 치료 옵션에 대한 의료적 수요가 매우 컸다"고 로슈 룬수미오의 활용성을 평가했다.마찬가지로 아주대병원 최윤석 교수(종양혈액내과)는 "개인적으로는 약간의 비대칭 전력이 된 것 같다. 다른 치료 옵션이 워낙 뒤처지는 측면이 있다"며 "DLBCL의 경우 CAR-T 치료제로 활용할 수 있는 것이 킴리아(티사젠렉류셀, 노바티스)인데 이후 활용할 수 있는 무기가 제한적이었다. 추가적인 옵션이 마련됐다"고 기대했다.국내 바이오 도전 속 '가격' 관심 아이큐비아에 따르면, 전 세계에서 약 130개 이중특이항체가 임상시험에 진입한 것으로 나타났다. 이 중 67%는 고형암, 24%는 혈액암이 적응증이다. 최근 혈액암 시장에서 신약이 출시돼 주목을 받고 있지만 고형암에서도 가능성을 엿보고 있는 셈이다. 국내 제약‧바이오업계에서도 에이비엘바이오 등을 필두로 이중특이항체를 주목하고 신약 개발에 도전 중이다. 에이비엘바이오의 경우 독자적인 이중항체 플랫폼을 토대로 다양한 파이프라인의 임상 개발을 추진하고 있는 가운데 ADC 기술에 대한 연구에도 적극적으로 나서고 있다. 이미 다수 기술이전으로 경쟁력을 입증한 이중항체에 ADC 기술을 접목한 '이중항체 ADC'를 활용한 파이프라인 개발에 집중하겠단 전략이다.여기에 최근 유한양행 자회사로 편입된 이뮨온시아도 이중특이항체 기반 항암제 개발을 위해 적극 나서고 있다. 와이바이오로직스와 이뮨온시아가 이중특이항체 기반 고형암 치료제 공동 개발을 위한 협약을 체결했다.최근 와이바이오로직스와 기존 PD-1 또는 PD-L1 항체가 불응하는 고형암에서 이중항체를 기반으로 한 치료제 개발을 위해 협력하기로 했다 개선하겠다는 목표를 세웠다. 앞서 이뮨온시아는 지난해 국제림프종학회(ICML 2023)에서 NK/T세포 림프종 환자를 대상으로 임상 2상을 진행 중인 'IMC-001'로 우수한 중간결과를 발표했다. 와이바이오로직스는 자체 이중항체 플랫폼을 활용해 신약후보 물질을 자체 개발하거나 국내외 파트너사들과 바이오 의약품을 공동 개발하고 있다.이뮨온시아 김흥태 대표(종양내과 전문의)는 "최근 글로벌 제약‧바이오 시장에서 주목받는 분야가 있다면 ADC와 이중특이항체 기반 치료제 개발"이라며 "ADC가 최근 들어 관심이 집중되고 있지만 이중특이항체의 경우 허가된 치료제들을 보면 상대적으로 치료제 안전성이 강점"이라고 강조했다.임상현장에서도 이 같은 국내 제약‧바이오 기업의 이중특이항체 기반 치료제 개발 움직임을 환영했다. 아주대병원 최윤석 교수는 "혈액암 분야에서 최근 이중특이항체 치료제가 각광을 받고 있는데 사실 CAR-T 치료제는 제한점이 크다. 국내에서 CAR-T 치료제를 활용할 수 있는 곳이 7개 의료기관 뿐"이라며 "상대적으로 이중특이항체 치료제는 이 같이 제한점이 없기 때문에 임상현장에서의 활용도가 클 수밖에 없다"고 말했다.그는 "국내 제약‧바이오기업이 개발 해내야 한다"며 "컬럼비나 룬수미오 등 글로벌 제약사 치료제는 결국 가격이 관건인데 신약 특성 상 글로벌 상황도 고려해 급여 적용 시 가격설정도 쉽지 않을 것 같다. 결과적으로 실손의료보험 등을 통해 환자들이 활용하는 형태가 현실화 될 것"이라고 예상했다.